Glutamin
| L-Glutamin | |||
|---|---|---|---|
 | |||
 | |||
| IUPAC ime |
| ||
| Drugi nazivi | 2-Amino-4-karbamoilbutanoinska kiselina | ||
| Identifikacija | |||
| Abrevijacija | Gln, Q | ||
| CAS registarski broj | 56-85-9  Y Y | ||
| PubChem[1][2] | 738 | ||
| ChemSpider[3] | 718 | ||
| EC-broj | 200-292-1 | ||
| MeSH | Glutamine | ||
| IUPHAR ligand | 723 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C5H10N2O3 | ||
| Molarna masa | 146.14 g mol−1 | ||
| Tačka topljenja | 185–186 °C (pazlaže se) | ||
| Rastvorljivost u vodi | rastvoran je | ||
| Hiralna rotacija [α]D | +6.5º (H2O, c = 2) | ||
| Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
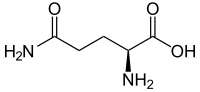
Glutamin (Gln, Q) je jedna od 20 amino kiselina koja je kodirana obrascem genetičkog koda. Njegov bočni lanac sadrži amidnu grupu, tako što je hidroksilna grupa glutaminske kiseline zamenjena sa amino grupom. Glutamin je u stvari monoamid glutaminske kiseline, a dobija se reakcijom glutaminske kiseline i amonijaka.[4][5]
Biohemija
Glutamin je genetički kodiran od strane RNK kodova CAA i CAG. Njegova troslovna skraćenica je Gln, a jednoslovna skraćenica Q. Troslovna oznaka za glutamin ili glutaminsku kiselinu je Glx (jednoslovna skraćenica je Z).
Kao i druge amino kiseline i glutamin je biohemijski važan sastojak proteina. Amonijak (nastao azotnom fiksacijom) je pretopljen u organska jedinjenja pretvaranjem glutaminske kiseline u glutamin. Enzim koji ovo omogućava se naziva glutamin sintaza. Glutamin, prema tome, može biti korišćen kao izvor azota u biosintezi mnogih jedinjenja, uključujući i druge amino kiseline, purine i pirimidine.
Ishrana
Glutamin se nalazi u hrani bogatoj proteinima, kao što je riba, crveno meso, pasulj i mlečni proizvodi. Glutamin se koristi kao pomoćno sredstvo kada se neko bavi dizanjem tegova, sportovima koji zahtevaju veću izdržljivost i nekim drugim sportovima, a isto tako ga koriste i oni koji pate od mišićnih grčeva ili reumatskih bolova. Osnovna namena za korišćenje glutamina sem u ishrani kod obe ove grupe, jeste i kao dodatak telesnim zalihama amino kiselina, jer su one bile korišćene tokom vežbanja ili svakodnevnih aktivnosti.[6][7]
Ispitivanja koja su istraživala probleme sa prekomernom potrošnjom glutamina do sad su se pokazala neubedljiva. Ipak, normalno doziranje je zdravo, prevashodno zato što bi glutamin trebao da se dodaje posle produženih perioda vežbanja (npr. treniranje ili vežbanje u kojem se zahteva korišćenje amino kiselina) kao i u ishrani u toku posta, i kod ljudi koji pate od psihičkih problema, oslabljenog imuniteta ili raka.
Postoji nekoliko ispitivanja koja govore o uticaju glutamina kao i o osobinama koje su osobene za njega. Danas postoji značajna količina dokaza koja povezuje glutaminom obogaćene dijete sa stvarima, kao što su: održavanje funkcije crevne bakterije, kao i to da generalno smanjuje septičnu bolešljivost i simptome problema sa varenjem.
Razlog za takve pročišćavajuće osobine koje poseduje glutamin, proizilaze iz činjenice da je intestinalna srazmera vađenja glutamina veća nego kod drugih amino kiselina i zbog toga se smatra najboljom opcijom kad se pokušavaju ublažiti problemi vezani za gastrointestinalni trakt.[8] Ovi uslovi su otkriveni posle poređenja koncentracije plazme u crevima između glutaminom obogaćene i neobogaćene dijete. Ipak, ako postoji mišljenje da glutamin ima pročišćavajuće osobine i uticaje, nepoznato je do kog opsega glutamin ima kliničke pogodnosti, zbog različitih koncentracija glutamina u raznovrsnoj ishrani.
Takođe je poznato da glutamin ima različite efekte u smanjivanju vremena zalečenja nakon operacija.[9] Vreme boravka u bolnici nakon operacije stomaka je značajno smanjeno jer se obezbeđuje propisan način ishrane pacijentima, koja sadrži određenu količnu glutamina. Klinička istraživanja su otkrila da pacijenti na režimu tekve dijete koja sadrži glutamin, imaju poboljšan azotni balans, generaciju cisteinil-leukotrienila iz polimorfnuklearnih neutrofilnih granulocita i poboljšan oporavak limfocija i intestinalnu permeabilnost (kod oprerisanih pacijenata), u poređenju sa onima koji nemaju glutamin u njihovom režimu ishrane, i sve to bez ikakvih sporednih efekata.
L-glutaminska kiselina je najzastupljenija amino kiselina u pšenici. Sadržana je u metabolizmu šećera i masti. Ima važnu ulogu za rad mozga, proizvodnju DNK, glutationa i ostalih amino kiselina. Pomaže odstranjenju amonijaka iz tela. L-glutamin je najvažniji izvor energije za mozak i celo telo. Ima ga u cerebralnom korteksu i drugim delovima mozga. Količina glutamina u krvi je tri do četiri puta veća od svih ostalih amino kiselina. Telo ga menja u glutaminsku kiselinu. Dokazano je da ima značajnu ulogu za pravilan rad imunološkog sistema.
Reference
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519. edit
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846. edit
- ↑ Darinka Koraćević, Gordana Bjelaković, Vidosava Đorđević. Biohemija. savremena administracija. ISBN 86-387-0622-7.
- ↑ David L. Nelson, Michael M. Cox (2005). Principles of Biochemistry (4th izd.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ↑ Boza J.J., Dangin M., Moennoz D., Montigon F., Vuichoud J., Jarret A., Pouteau E., Gremaud G., Oguey-Araymon S., Courtois D., Woupeyi A., Finot P.A. and Ballevre O. (2001). „Free and protein-bound glutamine have identical splanchnic extraction in healthy human volunteers.”. Am J Physiol Gastrointest Liver Physiol 281 (1): G267-74. PMID 11408280. Arhivirano iz originala na datum 2007-06-05. Pristupljeno 2010-04-06.
- ↑ McAnena O.J., Moore F.A., Moore E.E., Jones T.N. and Parsons P. (1991). „Selective uptake of glutamine in the gastrointestinal tract: confirmation in a human study”. Br J Surg 78 (4): 480-2. PMID 1903318.
- ↑ Jiang Z.M., Cao J.D., Zhu X.G., Zhao W.X., Yu J.C., Ma E.L., Wang X.R., Zhu M.W., Shu H., Liu Y.W. (1999). „The impact of alanyl-glutamine on clinical safety, nitrogen balance, intestinal permeability, and clinical outcome in postoperative patients: a randomised, double-blind, controlled study of 120 patients.”. JPEN J Parenter Enteral Nutr 23 (5): S62-6. PMID 10483898.
- ↑ Morlion B.J., Stehle P., Wachtler P., Siedhoff H.P., Koller M., Konig W., Furst P., Puchstein C. (1998). „Total parenteral nutrition with glutamine dipeptide after major abdominal surgery”. Ann Surg 227 (2): 302-8. PMID 9488531.
Literatura
Donald Voet, Judith G. Voet (2005). Biochemistry (3 izd.). Wiley. ISBN 978-0-471-19350-0.
Spoljašnje veze
 | Portal Hemija |

- Glutamine MS Spectrum
- p
- r
- u







