Acide periodique
| Acide periodique | |
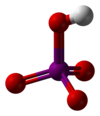 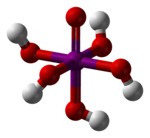 Structure des acides méta- et orthoperiodique. | |
| Identification | |
|---|---|
| Nom UICPA | acide periodique periodate d'hydrogène |
| No CAS | 10450-60-9 |
| No ECHA | 100.030.839 |
| No CE | 233-937-0 |
| PubChem | 25289 |
| Propriétés chimiques | |
| Formule | H5IO6 [Isomères] |
| Masse molaire[1] | 227,940 6 ± 0,002 2 g/mol H 2,21 %, I 55,67 %, O 42,11 %, |
| Propriétés physiques | |
| T° fusion | 122 °C[réf. souhaitée] |
| Précautions | |
| SIMDUT[2] | |
 C, C : Matière comburante cause ou favorise la combustion d'une autre matière en dégageant de l'oxygène Divulgation à 1,0% selon les critères de classification | |
| Directive 67/548/EEC | |
 C  O Symboles : C : Corrosif O : Comburant Phrases R : R8 : Favorise l’inflammation des matières combustibles. R34 : Provoque des brûlures. Phrases S : S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’eau et consulter un spécialiste. S45 : En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible, lui montrer l’étiquette). S36/37/39 : Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage. Phrases R : 8, 34, Phrases S : 26, 36/37/39, 45, | |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
L'acide periodique est la molécule HIO4 (acide métaperiodique) ou H5IO6 (acide orthoperiodique). Le nom de la molécule ne provient pas du mot « période », mais de « iode » : acide per-iodique (à comparer avec acide iodique ou acide perchlorique).
En solution diluée, l'acide periodique existe sous la forme d'ions H+ et IO4−. En concentration plus élevée, l'acide orthoperiodique, H5IO6, est formé. Celui-ci peut être obtenu sous forme cristalline.
Par chauffage sous pression réduite à 100 °C, l'acide orthoperiodique peut être déshydraté en acide métaperiodique, HIO4 :
- H5IO6 HIO4 + 2 H2O.
L'anhydride (heptoxyde de diiode, I2O7) ne peut être obtenu. En poursuivant le chauffage jusqu'à 150 °C environ, on obtient le pentoxyde de diiode (I2O5) :
- 2HIO4 → H2O + I2O5 + O2.
Voir aussi
Références
v · m | |
|---|---|
|
v · m | |
|---|---|
| Iodures I(-I) | |
| I(I) | |
| I(III) |
|
| I(V) |
|
| I(VII) |
|
 Portail de la chimie
Portail de la chimie












