| 2-méthylpentane |
 |
 |
| Représentations du 2-méthylpentane |
| Identification |
| DCI | 7892 |
| Nom UICPA | 2-méthylpentane |
| Synonymes | isohexane
diméthylpropylméthane |
| No CAS | 107-83-5 |
| No ECHA | 100.003.204 |
| No CE | 203-523-4 |
| PubChem | 7892 |
| SMILES | |
| InChI | InChI : vue 3D
InChI=1S/C6H14/c1-4-5-6(2)3/h6H,4-5H2,1-3H3
|
| Apparence | liquide incolore, d'odeur caractéristique[1] |
| Propriétés chimiques |
| Formule | C6H14 [Isomères]
|
| Masse molaire[2] | 86,175 4 ± 0,005 8 g/mol
C 83,63 %, H 16,37 %, |
| Propriétés physiques |
| T° fusion | −153 °C[1] |
| T° ébullition | 60,26 °C[3] |
| Solubilité | dans l'eau : nulle[1] |
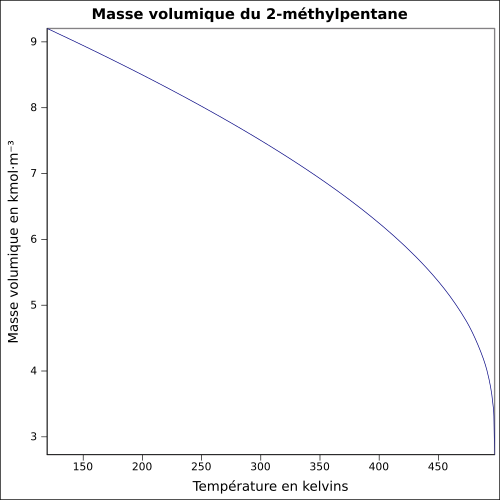
| Masse volumique |
équation[4] : 
Masse volumique du liquide en kmol·m-3 et température en kelvins, de 119,55 à 497,5 K.
Valeurs calculées :
0,6483 g·cm-3 à 25 °C. | T (K) | T (°C) | ρ (kmol·m-3) | ρ (g·cm-3) |
|---|
| 119,55 | −153,6 | 9,2041 | 0,79318 | | 144,75 | −128,4 | 8,98979 | 0,77471 | | 157,35 | −115,81 | 8,8805 | 0,76529 | | 169,94 | −103,21 | 8,76965 | 0,75574 | | 182,54 | −90,61 | 8,65714 | 0,74605 | | 195,14 | −78,01 | 8,54287 | 0,7362 | | 207,74 | −65,41 | 8,42671 | 0,72619 | | 220,34 | −52,81 | 8,30854 | 0,716 | | 232,94 | −40,22 | 8,18818 | 0,70563 | | 245,53 | −27,62 | 8,06549 | 0,69506 | | 258,13 | −15,02 | 7,94025 | 0,68427 | | 270,73 | −2,42 | 7,81226 | 0,67324 | | 283,33 | 10,18 | 7,68126 | 0,66195 | | 295,93 | 22,78 | 7,54696 | 0,65037 | | 308,53 | 35,38 | 7,40901 | 0,63849 | | | T (K) | T (°C) | ρ (kmol·m-3) | ρ (g·cm-3) |
|---|
| 321,12 | 47,97 | 7,26702 | 0,62625 | | 333,72 | 60,57 | 7,1205 | 0,61362 | | 346,32 | 73,17 | 6,96887 | 0,60056 | | 358,92 | 85,77 | 6,81144 | 0,58699 | | 371,52 | 98,37 | 6,64731 | 0,57285 | | 384,12 | 110,97 | 6,47538 | 0,55803 | | 396,71 | 123,56 | 6,29416 | 0,54241 | | 409,31 | 136,16 | 6,10171 | 0,52583 | | 421,91 | 148,76 | 5,89529 | 0,50804 | | 434,51 | 161,36 | 5,67088 | 0,4887 | | 447,11 | 173,96 | 5,42217 | 0,46727 | | 459,71 | 186,56 | 5,13824 | 0,4428 | | 472,3 | 199,15 | 4,79697 | 0,41339 | | 484,9 | 211,75 | 4,33767 | 0,37381 | | 497,5 | 224,35 | 2,729 | 0,23518 | |
|
| T° d'auto-inflammation | 264 °C[1] |
| Point d’éclair | −32 °C[1] |
| Limites d’explosivité dans l’air | 1,0–7 %vol[1] |
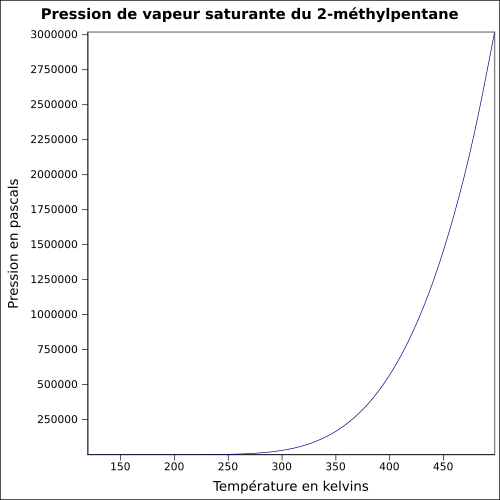
| Pression de vapeur saturante | à 20 °C : 23 kPa[1]
équation[4] : 
Pression en pascals et température en kelvins, de 119,55 à 497,5 K.
Valeurs calculées :
28 224,23 Pa à 25 °C. | T (K) | T (°C) | P (Pa) |
|---|
| 119,55 | −153,6 | 0 | | 144,75 | −128,4 | 0,01 | | 157,35 | −115,81 | 0,11 | | 169,94 | −103,21 | 0,9 | | 182,54 | −90,61 | 5,36 | | 195,14 | −78,01 | 24,46 | | 207,74 | −65,41 | 90,48 | | 220,34 | −52,81 | 281,84 | | 232,94 | −40,22 | 761,57 | | 245,53 | −27,62 | 1 827,82 | | 258,13 | −15,02 | 3 970,71 | | 270,73 | −2,42 | 7 927,59 | | 283,33 | 10,18 | 14 728,44 | | 295,93 | 22,78 | 25 725,88 | | 308,53 | 35,38 | 42 607,09 | | | T (K) | T (°C) | P (Pa) |
|---|
| 321,12 | 47,97 | 67 388,95 | | 333,72 | 60,57 | 102 400,29 | | 346,32 | 73,17 | 150 256,68 | | 358,92 | 85,77 | 213 833,63 | | 371,52 | 98,37 | 296 243,6 | | 384,12 | 110,97 | 400 821,17 | | 396,71 | 123,56 | 531 119,56 | | 409,31 | 136,16 | 690 920,33 | | 421,91 | 148,76 | 884 257,6 | | 434,51 | 161,36 | 1 115 456,99 | | 447,11 | 173,96 | 1 389 189,44 | | 459,71 | 186,56 | 1 710 540,02 | | 472,3 | 199,15 | 2 085 091,69 | | 484,9 | 211,75 | 2 519 024,69 | | 497,5 | 224,35 | 3 019 200 | |
 |
| Point critique | 3 032 kPa[5], 224,55 °C[3] |
| Thermochimie |
| ΔfH0gaz | 174,3 J·mol[6] |
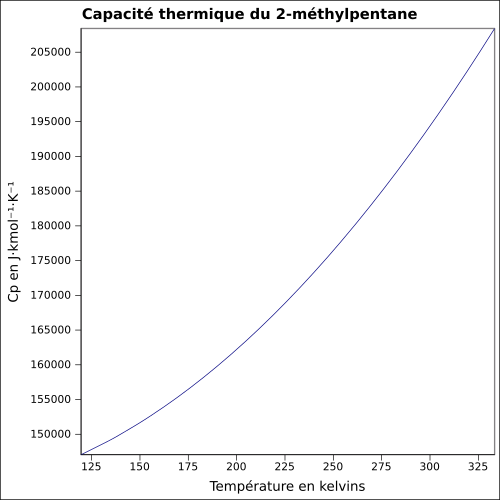
| Cp |
équation[4] : 
Capacité thermique du liquide en J·kmol-1·K-1 et température en kelvins, de 119,55 à 333,41 K.
Valeurs calculées :
193,652 J·mol-1·K-1 à 25 °C. T
(K) | T
(°C) | Cp
 | Cp
 |
|---|
| 119,55 | −153,6 | 147 060 | 1 707 | | 133 | −140,15 | 148 931 | 1 728 | | 140 | −133,15 | 150 008 | 1 741 | | 148 | −125,15 | 151 328 | 1 756 | | 155 | −118,15 | 152 561 | 1 770 | | 162 | −111,15 | 153 866 | 1 785 | | 169 | −104,15 | 155 243 | 1 801 | | 176 | −97,15 | 156 693 | 1 818 | | 183 | −90,15 | 158 215 | 1 836 | | 190 | −83,15 | 159 810 | 1 854 | | 197 | −76,15 | 161 477 | 1 874 | | 205 | −68,15 | 163 471 | 1 897 | | 212 | −61,15 | 165 294 | 1 918 | | 219 | −54,15 | 167 188 | 1 940 | | 226 | −47,15 | 169 156 | 1 963 | | T
(K) | T
(°C) | Cp
 | Cp
 |
|---|
| 233 | −40,15 | 171 195 | 1 987 | | 240 | −33,15 | 173 307 | 2 011 | | 247 | −26,15 | 175 492 | 2 036 | | 254 | −19,15 | 177 749 | 2 063 | | 262 | −11,15 | 180 416 | 2 094 | | 269 | −4,15 | 182 829 | 2 122 | | 276 | 2,85 | 185 313 | 2 150 | | 283 | 9,85 | 187 870 | 2 180 | | 290 | 16,85 | 190 499 | 2 211 | | 297 | 23,85 | 193 201 | 2 242 | | 304 | 30,85 | 195 975 | 2 274 | | 312 | 38,85 | 199 234 | 2 312 | | 319 | 45,85 | 202 164 | 2 346 | | 326 | 52,85 | 205 165 | 2 381 | | 333,41 | 60,26 | 208 420 | 2 419 | |
équation[7] : 
Capacité thermique du gaz en J·mol-1·K-1 et température en kelvins, de 200 à 1 500 K.
Valeurs calculées :
144,117 J·mol-1·K-1 à 25 °C. T
(K) | T
(°C) | Cp
 | Cp
 |
|---|
| 200 | −73,15 | 100 105 | 1 162 | | 286 | 12,85 | 138 951 | 1 612 | | 330 | 56,85 | 157 294 | 1 825 | | 373 | 99,85 | 174 272 | 2 022 | | 416 | 142,85 | 190 351 | 2 209 | | 460 | 186,85 | 205 913 | 2 389 | | 503 | 229,85 | 220 288 | 2 556 | | 546 | 272,85 | 233 875 | 2 714 | | 590 | 316,85 | 247 000 | 2 866 | | 633 | 359,85 | 259 102 | 3 007 | | 676 | 402,85 | 270 519 | 3 139 | | 720 | 446,85 | 281 528 | 3 267 | | 763 | 489,85 | 291 660 | 3 384 | | 806 | 532,85 | 301 205 | 3 495 | | 850 | 576,85 | 310 394 | 3 602 | | T
(K) | T
(°C) | Cp
 | Cp
 |
|---|
| 893 | 619,85 | 318 840 | 3 700 | | 936 | 662,85 | 326 786 | 3 792 | | 980 | 706,85 | 334 428 | 3 881 | | 1 023 | 749,85 | 341 446 | 3 962 | | 1 066 | 792,85 | 348 044 | 4 039 | | 1 110 | 836,85 | 354 388 | 4 112 | | 1 153 | 879,85 | 360 213 | 4 180 | | 1 196 | 922,85 | 365 692 | 4 244 | | 1 240 | 966,85 | 370 962 | 4 305 | | 1 283 | 1 009,85 | 375 806 | 4 361 | | 1 326 | 1 052,85 | 380 369 | 4 414 | | 1 370 | 1 096,85 | 384 766 | 4 465 | | 1 413 | 1 139,85 | 388 818 | 4 512 | | 1 456 | 1 182,85 | 392 646 | 4 556 | | 1 500 | 1 226,85 | 396 348 | 4 599 | |
|
| Précautions |
| Directive 67/548/EEC |
Numéro index :
601-007-00-7
Classification :
F; R11 - Xn; R65 - Xi; R38 - R67 - N; R51-53
Symboles :
Xn : Nocif
F : Facilement inflammable
N : Dangereux pour l’environnement
Phrases R :
R11 : Facilement inflammable.
R38 : Irritant pour la peau.
R51 : Toxique pour les organismes aquatiques.
R53 : Peut entraîner des effets néfastes à long terme pour l’environnement aquatique.
R65 : Nocif : peut provoquer une atteinte des poumons en cas d’ingestion.
Phrases S :
S2 : Conserver hors de portée des enfants.
S9 : Conserver le récipient dans un endroit bien ventilé.
S16 : Conserver à l’écart de toute flamme ou source d’étincelles - Ne pas fumer.
S29 : Ne pas jeter les résidus à l’égout.
S33 : Éviter l’accumulation de charges électrostatiques.
S61 : Éviter le rejet dans l’environnement. Consulter les instructions spéciales/la fiche de données de sécurité.
S62 : En cas d’ingestion, ne pas faire vomir. Consulter immédiatement un médecin et lui montrer l’emballage ou l’étiquette.
|
|
| Unités du SI et CNTP, sauf indication contraire. |
modifier  |








 Portail de la chimie
Portail de la chimie 
















